从药品集采质量要求谈基毒类杂质研究的重要意义
时间:2023/3/2 20:25:49 来源:本站
7月18日,国家组织药品联合采购办公室发布《关于公布全国药品集中采购(GY-YD2022-1)中选结果的通知》,第七批集采共有295家企业的488个产品参与投标,最终217家企业的327个产品获得中选资格,投标品种中选比例约为67%。集采既降低了患者的用药负担,也成为了一些企业拓展市场的机会,那么对于研发人员而言,从这次集采中又能获得哪些启示呢?
根据本次国联采字〔2022〕1号《全国药品集中采购文件(GY-YD2022-1)》的公告,结合近三年发布的全国药品集中采购文件,申报资格中均要求企业所申报的药品“应当符合国家药品标准和经国家药品监督管理部门核准的药品质量标准,并按照国家药品监督管理局药品审评中心关于发布《化学药物中亚硝胺类杂质研究技术指导原则(试行)》的通告(2020年1号)组织生产”。从中不难看出,近年来随着药品质量标准和安全性评价要求的不断提升,基因毒性杂质检测引发业界关注,亚硝胺类物质已属于医药行业目前重点关注的一类杂质。本文将回顾亚硝胺类杂质在国内外引起关注的历程,同时结合峰林生物的研究平台探讨基因毒性杂质的研究意义。
一、亚硝胺类杂质背景介绍
2018年7月在缬沙坦原料药中检出N-亚硝基二甲胺(NDMA),此后陆续在其他沙坦类原料药(氯沙坦、厄贝沙坦)中也检出了NDMA和N-亚硝基二乙胺(NDEA)等各类亚硝胺杂质。进一步的调查发现,在个别供应商的非沙坦类的药物(如雷尼替丁、二甲双胍和盐酸吡格列酮)中,亦有亚硝胺类杂质的检出。亚硝胺类杂质属于ICH M7(R1)(《评估和控制药物中DNA反应性(致突变)杂质以限制潜在的致癌风险》)指南中提及的“关注队列”物质。根据世界卫生组织公布的致癌物清单(见表1),NDMA和NDEA均属于2A类致癌物质。FDA已经确定了7种理论上可能存在于药品中的亚硝胺类杂质:NDMA、NDEA、N-亚硝基-N-甲基-4-氨基丁酸(NMBA)、N-亚硝基二丁胺(NDBA)、N-亚硝基异丙基乙胺(NIPEA)、N-亚硝基二异丙胺(NDPA)、N-亚硝基甲基苯胺(NMPA),其中NDMA、NDEA、NMBA、NIPEA和NMPA这5种已经在相关原料药或药品中检出。
表1 世界卫生组织国际癌症研究机构致癌物清单(亚硝胺类)
二、亚硝胺类杂质产生的原因
国家药品监督管理局药品审评中心分别于2019年1月14日和2020年5月8日,发布了公开征求《关于在原料药工艺中生成亚硝胺类化合物的风险警示》意见的通知和关于发布《化学药物中亚硝胺类杂质研究技术指导原则(试行)》的通告(2020年第1号),明确表示胺类化合物,尤其是仲胺,在与亚硝酸钠(NaNO2)或其他亚硝化试剂反应后会产生亚硝胺类杂质,生成途径如下所示。
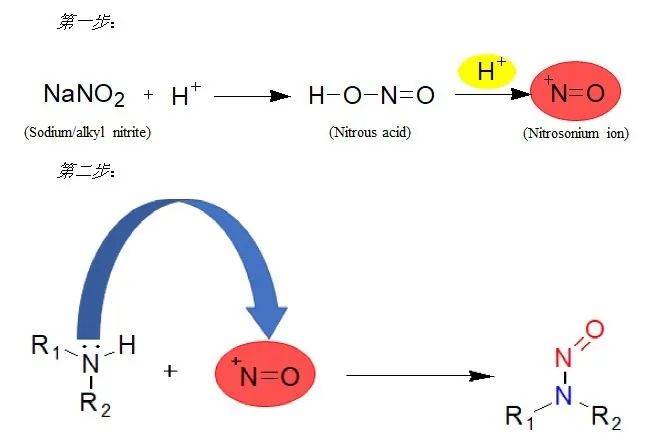
仲胺来源:除物料本身带有仲胺结构外,可能的仲胺来源还包括伯胺、叔胺及季铵中存在的仲胺杂质,以及酰胺类溶剂(如N,N-二甲基甲酰胺、N-甲基吡咯烷酮等)在适宜条件下(如:酸性,高温等)产生的仲胺。亚硝化试剂来源:亚硝酸盐、亚硝酸酯、亚硝酸,由亚硝酸盐制备的物质(如叠氮化钠等),以及胺类化合物的氧化等。在同一工艺步骤中使用能引入仲胺和亚硝化试剂的物料(包括起始物料、溶剂、试剂、催化剂、中间体等),将有较高的风险产生亚硝胺类杂质。即使在不同的工艺步骤中分别使用能引入仲胺和亚硝化试剂的物料,也可能会产生亚硝胺类杂质。原料药生产过程中使用了被亚硝胺类杂质污染的物料(包括起始物料、中间体、溶剂、试剂、催化剂等)可能带来引入亚硝胺类杂质的风险。使用回收的物料亦有引入亚硝胺类杂质的风险,已发现的回收物料被亚硝胺污染的实例包括邻二甲苯、氯化三丁基锡(用作叠氮化三丁基锡的来源)、N,N-二甲基甲酰胺(DMF)。在同一生产线生产不同的品种,交叉污染也可能成为引入亚硝胺类杂质的潜在原因。某些药物本身会降解产生亚硝胺类杂质,如2019年9月在雷尼替丁中发现了杂质NDMA,葛兰素史克公司通过同位素标记法发现NDMA来源于药物结构中的硝基和二甲胺反应,并且随着时间的推移NDMA会不断地增加。
在研发阶段根据亚硝胺类杂质产生的原因,对原料药工艺路线、物料(包括起始物料、溶剂、试剂、催化剂、中间体等)、工艺条件及生产过程等方面按照ICH Q9或其他科学合理的方法,进行系统的风险评估。若评估发现有生成亚硝胺类杂质的风险,应首先分析亚硝化试剂等相关物料在工艺中使用的必要性,尽量避免选择可能生成亚硝胺类杂质的生产工艺。若具有亚硝胺类杂质残留风险且相关工艺无法避免时,应尽可能将该步骤调整至工艺的早期,通过后续多步骤的操作降低亚硝胺类杂质的残留风险。同时根据工艺路线分析可能生成的亚硝胺结构,优化工艺,增加适宜的杂质清除步骤,制定详细的过程控制策略,保证生产过程中此类杂质的有效去除。若评估发现亚硝胺类杂质是由降解产生,则应分析降解产生的条件,通过优化生产工艺、处方、贮存条件等,降低降解杂质产生的风险。在药品开发阶段,对物料(包括原料药、辅料、包材等)、工艺及生产过程等方面,按照ICH Q9或其他科学合理的方法,进行系统的风险评估。若评估发现有生成亚硝胺类杂质的风险,需要和物料厂家进行充分沟通,识别确定杂质来源,才有可能保证不同批次间的产品杂质水平较为一致,风险可控。应从制剂处方、生产工艺、贮存条件等方面进行控制,建立内控标准和合适的分析方法,对成品和稳定性期间样品进行检测,确保制剂中亚硝胺类杂质低于相关限度要求。根据研发品种的物料属性、工艺路线、生产过程、降解情况、分析测试结果与监管机构的要求确定应该控制的亚硝胺类杂质种类。亚硝胺类杂质的致癌风险较高,参考ICH M7指南的相关规定以及国际权威机构(如WHO、国际化学品安全性方案、FDA、EMA等)推荐的TD50数据,制定控制策略。未在权威机构库中查见TD50值的亚硝胺类杂质,若与已有TD50值的亚硝胺类杂质结构相似,可以导用其TD50值计算杂质限度。FDA推荐的6种亚硝胺类杂质(NDMA、NDEA、NMBA、NMPA、NIPEA、NDIPA)可接受摄入限值见下表:
亚硝胺类杂质的每日可接受摄入量
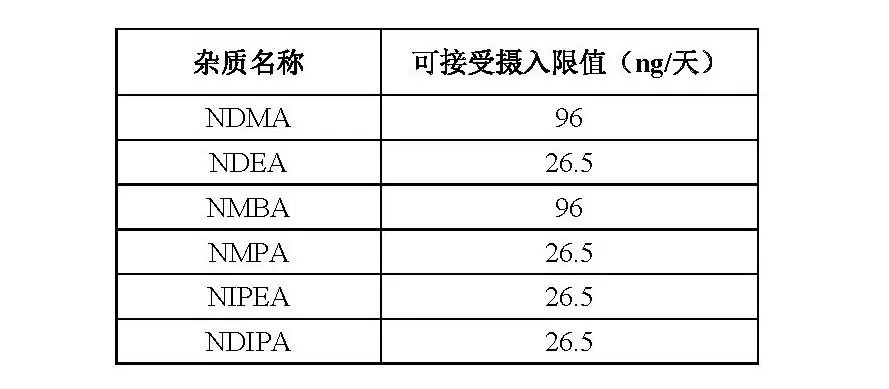
例:NDMA的每日最大摄入量为96ng/天。若按照缬沙坦每日最大用药320mg计算,则其NDMA限度设定为:96ng/320mg=0.00003%=0.30ppm。《美国药典》通则<1469> NITROSAMINE IMPURITIES于2021年12月1日正式实施,该通则为亚硝胺类杂质提供了一种科学的风险控制方法。该通则章节中提出了四种分析方法,制药商可以使用这些方法来鉴别其产品中是否存在亚硝胺类杂质。第一种方法是高效液相色谱-高分辨率质谱(HPLC-HRMS),推荐用于检测NDMA、NDEA、NDIPA、NEIPA、NMBA和NDBA,样品通常用甲醇涡旋溶解或分散。第二种方法是气相色谱-质谱(GC-MS),推荐用于检测NDMA、NDEA、NDIPA和NEIPA,样品通常用乙腈/咪唑溶解。第三种方法是高效液相色谱-串联质谱(HPLC-MS/MS),推荐用于NDMA、NDEA、NDIPA、NEIPA、NMBA和NDBA,样品通常用甲酸水溶液或甲酸甲醇溶液溶解。第四种方法是气相色谱-串联质谱(GC-MS/MS),推荐用于NDMA、NDEA、NDIPA、NEIPA和NDBA,样品通常用二氯甲烷提取。由于某些药物热稳定性较差,加热后会产生高水平的亚硝胺类杂质,故液相色谱-质谱联用方法比气相色谱-质谱法更具适用性。
上海峰林生物科技有限公司始终秉持创新、诚信、共赢、责任的理念,在基因毒性杂质研究方面紧跟行业规范的最新要求,建立了基因毒性杂质研究平台。平台拥有安捷伦1290型高效液相色谱仪与6470型三重四极杆质谱仪等仪器,可以提供基于HPLC-串联质谱(HPLC-MS/MS)的基因毒性杂质研究与分析检测服务。公司成立至今已完成了如磺酸酯类、氨基甲酸酯类、磷酸酯类、氯乙酸酯、卤代烃类、肼类、芳香胺(醛)、氯乙酰胺、脂肪醛、吖啶、吖酮类等近百种杂质的研究,确保了患者的用药安全。
峰林生物 6470型三重四极杆质谱仪
|
研究示例
亚硝胺类等基因毒性杂质具有浓度低、种类多的特点,方法开发与验证的关键点在于专属性、灵敏度与精密度。测试结果表明NDMA和NDEA的专属性、灵敏度与重复性良好。
|
结语
随着人们对于亚硝胺类等各种基因毒性杂质产生机理认识的不断更新,检测技术的不断进步,以及各类政策法规和监管制度的不断完善,需要广大医药研发人员既要脚踏实地,提升对于产品特性的认知,也要抬头看路,持续关注行业的评判准则,这样才能保证药品的安全、有效和质量可控。



